Para baixar ou imprimir esta página em um idioma diferente, escolha primeiro seu idioma no menu suspenso no canto superior esquerdo.

Documento de posição da IAOMT sobre cavitações do maxilar humano
Presidente do Comitê de Patologia do Maxilar: Ted Reese, DDS, MAGD, NMD, FIAOMT
Karl Anderson, DDS, MS, NMD, FIAOMT
Patricia Berube, DMD, MS, CFMD, FIAOMT
Jerry Bouquot, DDS, MSD
Teresa Franklin, PhD
Jack Kall, DMD, FAGD, MIAOMT
Cody Kriegel, DDS, NMD, FIAOMT
Sushma Lavu, DDS, FIAOMT
Tiffany Shields, DMD, NMD, FIAOMT
Mark Wisniewski, DDS, FIAOMT
A comissão gostaria de expressar o nosso agradecimento a Michael Gossweiler, DDS, MS, NMD, Miguel Stanley, DDS e Stuart Nunally, DDS, MS, FIAOMT, NMD pelas suas críticas a este artigo. Gostaríamos também de reconhecer as contribuições e o esforço inestimáveis feitos pelo Dr. Nunnally na compilação do documento de posição de 2014. Seu trabalho, diligência e prática forneceram a espinha dorsal para este artigo atualizado.
Aprovado pelo Conselho de Administração da IAOMT em setembro de 2023
Índice
Tomografia computadorizada de feixe cônico (TCFC)
Biomarcadores e exame histológico
Considerações em evolução para fins de diagnóstico
Avaliação do Meridiano de Acupuntura
Implicações sistêmicas e clínicas
Estratégias alternativas de tratamento
Referências
Apêndice I Resultados da Pesquisa IAOMT 2
Apêndice II Resultados da Pesquisa IAOMT 1
Apêndice III Imagens
Figura 1 Osteonecrose degenerativa gordurosa do maxilar (FDOJ)
Figura 2 Citocinas em FDOJ em comparação com controles saudáveis
Figura 3 Procedimento cirúrgico para FDOJ retromolar
Figura 4 Curetagem e radiografia correspondente do FDOJ
Filmes Videoclipes de cirurgia de maxilar em pacientes
Ao longo da última década tem havido uma consciencialização crescente entre o público e os prestadores de cuidados de saúde relativamente à ligação entre a saúde oral e a saúde sistémica. Por exemplo, a doença periodontal é um fator de risco tanto para diabetes como para doenças cardíacas. Uma ligação potencialmente consequente e cada vez mais pesquisada também foi demonstrada entre a patologia do maxilar e a saúde e vitalidade geral do indivíduo. O uso de modalidades de imagem tecnicamente avançadas, como a tomografia computadorizada de feixe cônico (TCFC), tem sido fundamental na identificação de patologias do maxilar, o que levou a melhores capacidades de diagnóstico e a uma melhor capacidade de avaliar o sucesso de intervenções cirúrgicas. Relatórios científicos, docudramas e meios de comunicação social aumentaram a sensibilização do público para estas patologias, especialmente entre aqueles indivíduos que sofrem de condições neurológicas ou sistémicas crónicas inexplicáveis que não respondem às intervenções médicas ou dentárias tradicionais.
A Academia Internacional de Medicina Oral e Toxicologia (IAOMT) baseia-se na crença de que a ciência deve ser a base sobre a qual todas as modalidades de diagnóstico e tratamento devem ser escolhidas e utilizadas. É com essa prioridade em mente que 1) fornecemos esta atualização ao nosso documento de posição sobre osteonecrose do maxilar da IAOMT de 2014 e 2) propomos, com base na observação histológica, um nome mais científico e médico preciso para a doença, especificamente, Doença Medular Isquêmica Crônica do Maxilar (CIMDJ). CIMDJ descreve uma condição óssea caracterizada pela morte de componentes celulares do osso esponjoso, secundária a uma interrupção do suprimento sanguíneo. Ao longo da sua história, aquilo a que nos referimos como CIMDJ foi referido por uma infinidade de nomes e siglas que estão listados na Tabela 1 e serão brevemente discutidos abaixo.
O objetivo e a intenção desta Academia e do artigo é fornecer ciência, pesquisa e observações clínicas para que pacientes e médicos tomem decisões informadas ao considerar essas lesões CIMDJ, que são frequentemente chamadas de cavitações do maxilar. Este artigo de 2023 foi elaborado em um esforço conjunto que incluiu médicos, pesquisadores e um eminente patologista maxilar, Dr. Jerry Bouquot, após revisão de mais de 270 artigos.
Em nenhum outro osso o potencial para traumas e infecções é tão grande quanto nos maxilares. Uma revisão da literatura relativa ao tema das cavitações maxilares (isto é, CIMDJ) mostra que esta condição tem sido diagnosticada, tratada e pesquisada desde a década de 1860. Em 1867, o Dr. HR Noel fez uma apresentação intitulada Palestra sobre cárie e necrose óssea no Baltimore College of Dental Surgery, e em 1901 as cavitações do maxilar são discutidas detalhadamente por William C. Barrett em seu livro intitulado Oral Pathology and Practice: A Textbook for the Use of Students in Dental Colleges and a Handbook for Dental Practitioners. GV Black, muitas vezes referido como o pai da odontologia moderna, incluiu uma seção em seu livro de 1915, Special Dental Pathology, para descrever “a aparência usual e o tratamento” do que ele descreveu como osteonecrose do maxilar (JON).
A pesquisa sobre cavitações maxilares pareceu parar até a década de 1970, quando outros começaram a pesquisar o assunto, usando uma variedade de nomes e rótulos, e publicando informações a respeito em livros modernos de patologia bucal. Por exemplo, em 1992, Bouquot et al observaram inflamação intraóssea em pacientes com dor facial crônica e intensa (N = 135) e cunharam o termo 'Osteonecrose Cavitacional Indutora de Neuralgia', ou NICO. Embora Bouquot et al não tenham comentado a etiologia da doença, concluíram que era provável que as lesões induzissem uma neuralgia facial crônica com características locais únicas: formação de cavidade intraóssea e necrose óssea de longa data com cicatrização mínima. Em um estudo clínico com pacientes com neuralgia do trigêmeo (N=38) e facial (N=33), Ratner et al, também mostraram que quase todos os pacientes apresentavam cáries no osso alveolar e na mandíbula. As cáries, às vezes com mais de 1 centímetro de diâmetro, estavam nos locais de extrações dentárias anteriores e geralmente não eram detectáveis por raios X.

 Uma variedade de outros termos para o que identificamos como CIMDJ existe na literatura. Eles estão listados na Tabela 1 e discutidos brevemente aqui. Adams et al cunharam o termo Osteomielite Fibrosante Crônica (CFO) em um documento de posicionamento de 2014. O documento de posicionamento foi resultado de um consórcio multidisciplinar de profissionais das áreas de Medicina Oral, Endodontia, Patologia Oral, Neurologia, Reumatologia, Otorrinolaringologia, Periodontia, Psiquiatria, Radiologia Oral e Maxilofacial, Anestesia, Odontologia Geral, Medicina Interna e Tratamento da Dor. . O foco do grupo era fornecer uma plataforma interdisciplinar para tratar doenças associadas à cabeça, pescoço e face. Através dos esforços coletivos deste grupo, extensas pesquisas bibliográficas e entrevistas com pacientes, emergiu um padrão clínico distinto, que eles chamaram de CFO. Eles observaram que esta doença muitas vezes não é diagnosticada devido às suas comorbidades com outras condições sistêmicas. Este grupo destacou as potenciais ligações entre a doença e problemas de saúde sistémicos e a necessidade de uma equipa de médicos para diagnosticar e tratar adequadamente o paciente.
Uma variedade de outros termos para o que identificamos como CIMDJ existe na literatura. Eles estão listados na Tabela 1 e discutidos brevemente aqui. Adams et al cunharam o termo Osteomielite Fibrosante Crônica (CFO) em um documento de posicionamento de 2014. O documento de posicionamento foi resultado de um consórcio multidisciplinar de profissionais das áreas de Medicina Oral, Endodontia, Patologia Oral, Neurologia, Reumatologia, Otorrinolaringologia, Periodontia, Psiquiatria, Radiologia Oral e Maxilofacial, Anestesia, Odontologia Geral, Medicina Interna e Tratamento da Dor. . O foco do grupo era fornecer uma plataforma interdisciplinar para tratar doenças associadas à cabeça, pescoço e face. Através dos esforços coletivos deste grupo, extensas pesquisas bibliográficas e entrevistas com pacientes, emergiu um padrão clínico distinto, que eles chamaram de CFO. Eles observaram que esta doença muitas vezes não é diagnosticada devido às suas comorbidades com outras condições sistêmicas. Este grupo destacou as potenciais ligações entre a doença e problemas de saúde sistémicos e a necessidade de uma equipa de médicos para diagnosticar e tratar adequadamente o paciente.
Lesões cavitacionais do maxilar também foram observadas em crianças. Em 2013, Obel et al descreveram lesões em crianças e cunharam o termo Osteomielite Crônica Mandibular Juvenil (JMCO). Este grupo sugeriu o possível uso de bifosfonatos intravenosos (IV) como tratamento para essas crianças. Em 2016, Padwa et al publicaram um estudo descrevendo uma osteíte inflamatória estéril focal em maxilares de pacientes pediátricos. Eles rotularam a lesão Osteomielite Não Bacteriana Crônica Pediátrica (CNO).
Desde 2010, o Dr. Johann Lechner, o autor e pesquisador mais amplamente publicado em lesões cavitacionais do maxilar, e outros têm pesquisado a relação dessas lesões com a produção de citocinas, especialmente a citocina inflamatória RANTES (também conhecida como CCL5). Lechner usou vários termos para descrever essas lesões, que incluíram o NICO mencionado anteriormente, mas também Osteonecrose Isquêmica Asséptica no Maxilar (AIOJ) e Osteonecrose Degenerativa Gordurosa do Maxilar (FDOJ). Sua descrição/rótulo é baseada na aparência física e/ou na condição macroscopicamente patológica observada clínica ou intraoperatoriamente.
Existe agora a necessidade de esclarecer outra patologia óssea maxilar identificada mais recentemente, que é distinta do tópico deste artigo, mas que pode ser confusa para aqueles que pesquisam lesões cavitacionais. São lesões ósseas da mandíbula que surgem como resultado do uso de produtos farmacêuticos. As lesões são melhor caracterizadas pela perda de suprimento sanguíneo com subsequente sequestro ósseo incontrolável. Estas lesões foram denominadas Ulceração Oral com Sequestro Ósseo (OUBS) por Ruggiero et al em um documento de posição para Associação Americana de Cirurgiões Orais e Maxilofaciais (AAOMS), bem como por Palla et al, em revisão sistemática. Uma vez que este problema está relacionado com o uso de um ou vários produtos farmacêuticos, a IAOMT considera que este tipo de lesão é melhor descrito como Osteonecrose da Mandíbula Relacionada com Medicamentos (MRONJ). MRONJ não será discutido neste artigo porque sua etiologia e abordagens de tratamento são diferentes daquelas que chamamos de CIMDJ, e já foi extensivamente estudada anteriormente.
O uso cada vez mais comum de radiografias de tomografia computadorizada de feixe cônico (TCFC) por muitos dentistas levou a um aumento na observância das cavitações intramedulares que chamamos de CIMDJ, e que antes eram negligenciadas e, portanto, ignoradas. Agora que essas lesões e anomalias são mais facilmente identificadas, torna-se responsabilidade da profissão odontológica diagnosticar a doença e fornecer recomendações de tratamento e cuidados.
Apreciar e identificar a existência do CIMDJ é o ponto de partida para a sua compreensão. Independentemente dos muitos nomes e siglas associados à patologia, a presença de osso necrótico ou moribundo no componente medular do maxilar está bem estabelecida.
Quando observados durante a cirurgia, esses defeitos ósseos apresentam-se de diversas maneiras. Alguns médicos relatam que mais de 75% das lesões são completamente ocas ou preenchidas com tecido macio, marrom-acinzentado e desmineralizado/granulomatis, muitas vezes com material oleoso amarelo (cistos oleosos) encontrado nas áreas defeituosas com anatomia óssea normal circundante. Outros relatam a presença de cavitações com densidade óssea cortical variável que, após a abertura, parecem ter revestimentos com materiais filamentosos fibrosos pretos, marrons ou cinza. Outros ainda relatam alterações grosseiras descritas como “arenosas”, “semelhantes a serragem”, “cavidades ocas” e “secas”, com ocasionalmente esclerótica, dureza semelhante a um dente nas paredes da cavidade. Ao exame histológico, essas lesões parecem semelhantes à necrose que ocorre em outros ossos do corpo e são histologicamente diferentes da osteomielite (ver Figura 1). Imagens adicionais que ilustram a doença CIMDJ, algumas de natureza gráfica, estão incluídas no Apêndice III no final deste documento.
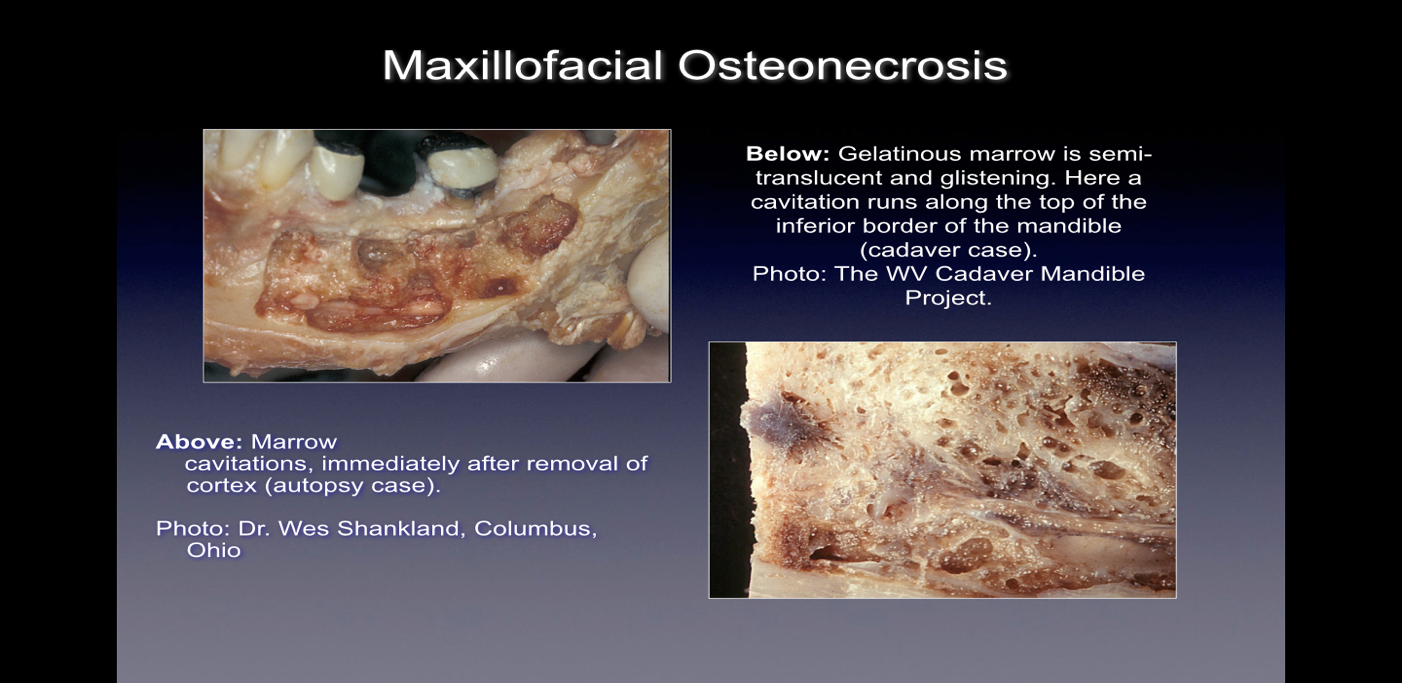
Figura 1 Imagens do CIMDJ retiradas de cadáver
Como outros profissionais de saúde, os dentistas utilizam um processo organizado que utiliza vários métodos e modalidades para diagnosticar lesões cavitacionais. Estes podem consistir na realização de um exame físico que inclui a obtenção de um histórico de saúde, avaliação de sintomas, obtenção de fluidos corporais para realização de exames laboratoriais e obtenção de amostras de tecido para biópsia e testes microbiológicos (isto é, testes para a presença de patógenos). Tecnologias de imagem, como CBCT, também são frequentemente utilizadas. Em pacientes com distúrbios complexos que nem sempre seguem um padrão ou se enquadram na ordem típica de um complexo de sintomas, o processo diagnóstico pode exigir uma análise mais detalhada que, a princípio, pode resultar apenas em um diagnóstico diferencial. Breves descrições de várias dessas modalidades de diagnóstico são fornecidas abaixo.
Tomografia computadorizada de feixe cônico (TCFC)
Técnicas diagnósticas descritas já em 1979 por Ratner e colegas, utilizando palpação e pressões digitais, injeções diagnósticas de anestésicos locais, consideração de históricos médicos e localização da dor irradiada são úteis no diagnóstico de cavitações ósseas maxilares. No entanto, enquanto algumas destas lesões causam dor, inchaço, vermelhidão e até febre, outras não. Assim, muitas vezes é necessária uma medida mais objetiva, como a imagem.
As cavitações geralmente não são detectadas em filmes radiográficos bidimensionais padrão (2-D, como periapicais e panorâmicos) comumente usados em odontologia. Ratner e colegas demonstraram que 40% ou mais do osso precisa ser alterado para mostrar alterações, e isso é apoiado por trabalhos posteriores, e ilustrado na Figura 2. Isto está relacionado à limitação inerente da imagem 2-D que causa sobreposição de estruturas anatômicas, mascarando áreas de interesse. No caso de defeitos ou patologias, especificamente na mandíbula, o efeito de mascaramento do osso cortical denso nas estruturas subjacentes pode ser significativo. Portanto, são necessárias técnicas de imagem tecnologicamente avançadas, como TCFC, exames Tech 99, ressonância magnética (MRI) ou ultrassonografia transalveolar (CaviTAU™®) .
Das diversas técnicas de imagem disponíveis, a TCFC é a ferramenta de diagnóstico mais utilizada pelos dentistas envolvidos no diagnóstico ou tratamento de cavitações e, portanto, aquela que discutiremos em profundidade. A pedra angular da tecnologia CBCT é a sua capacidade de visualizar uma lesão de interesse em 3 dimensões (frontal, sagital, coronal). A TCFC provou ser um método confiável e preciso para identificar e estimar o tamanho e a extensão de defeitos intraósseos na mandíbula, com menos distorção e menor ampliação do que as radiografias 2D.
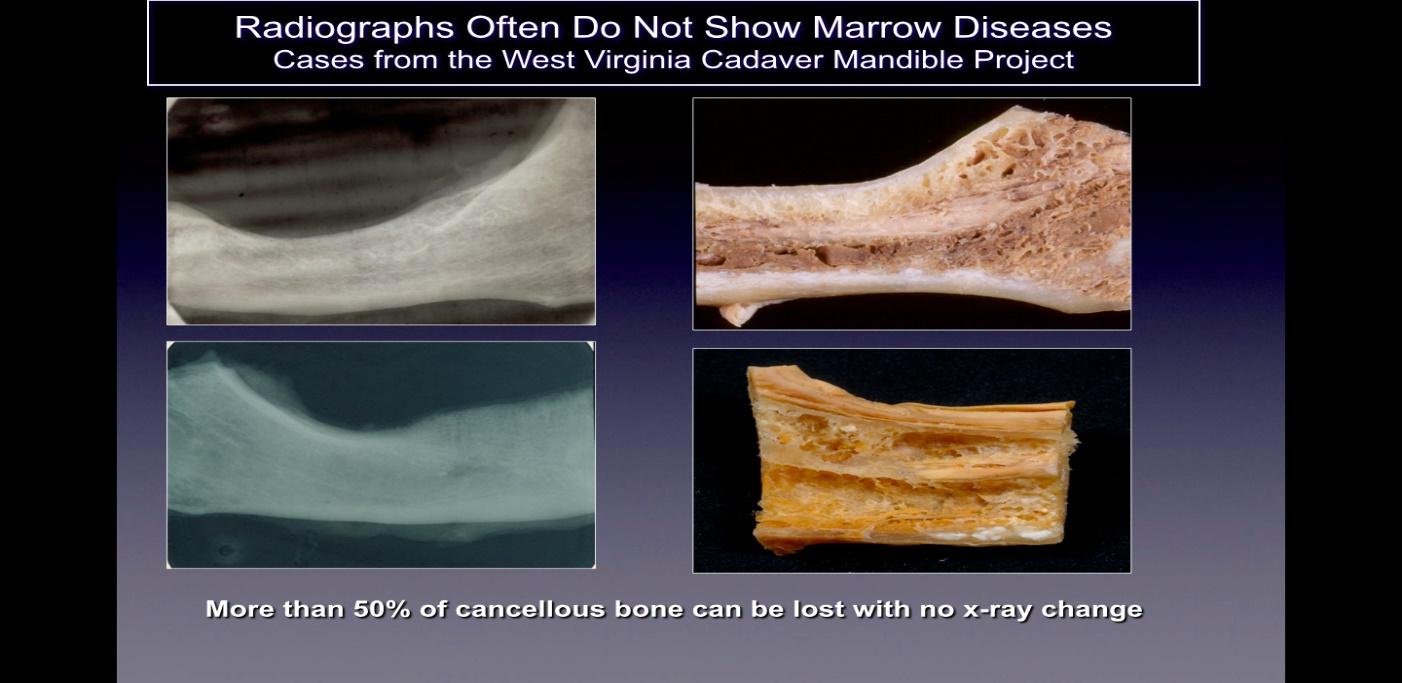
Figura 2 Legenda: No lado esquerdo são mostradas radiografias 2-D de maxilares retiradas de cadáveres que aparecem
saudável. No lado direito da figura estão fotografias dos mesmos maxilares mostrando evidente cavitação necrótica.
Figura adaptada de Bouquot, 2014.
Estudos clínicos demonstraram que as imagens de TCFC também auxiliam na determinação do conteúdo de uma lesão (cheia de líquido, granulomatosa, sólida, etc.), possivelmente ajudando a distinguir entre lesões inflamatórias, tumores odontogênicos ou não odontogênicos, cistos e outros tumores benignos ou malignos. lesões.
O software recentemente desenvolvido que é especificamente integrado com diferentes tipos de dispositivos de TCFC utiliza unidades Hounsfield (HU), que permitem uma avaliação padronizada da densidade óssea. HU representa a densidade relativa dos tecidos corporais de acordo com uma escala calibrada de nível de cinza, com base em valores de ar (-1000 HU), água (0 HU) e densidade óssea (+1000 HU). A Figura 3 mostra diferentes visualizações de uma imagem moderna de TCFC.
Resumindo, a TCFC provou ser útil no diagnóstico e tratamento de cavitações ósseas:
- Identificar o tamanho, extensão e posição 3D de uma lesão;
- Identificar a proximidade de uma lesão com outras estruturas anatômicas vitais próximas, como o
nervo alveolar inferior, seio maxilar ou raízes dentárias adjacentes;
- Determinar a abordagem de tratamento: cirúrgico versus não cirúrgico; e
- Fornecer uma imagem de acompanhamento para determinar o grau de cura e a possível necessidade
para tratar novamente uma lesão.
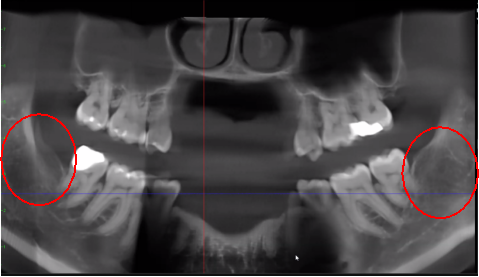
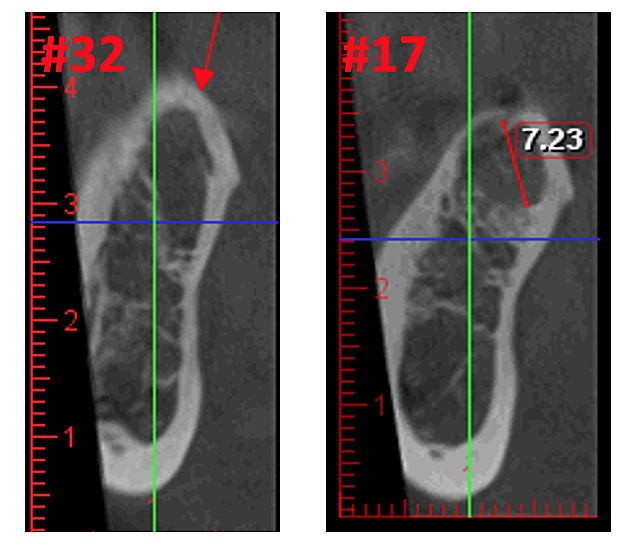
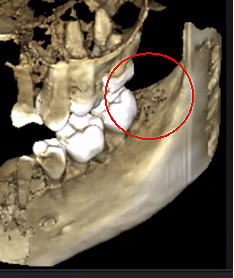
Figura 3 Maior clareza da imagem CBCT devido à tecnologia de software refinada, que reduz artefatos e “ruídos” que implantes dentários e restaurações metálicas podem causar na imagem. Isso permite que o dentista e o paciente visualizem a lesão com mais facilidade. O painel superior é uma vista panorâmica de uma TCFC mostrando a localização e extensão das lesões cavitacionais à esquerda (#17) e à direita (#32) em um paciente com osteonecrose do maxilar. O painel inferior esquerdo é uma visão sagital de cada site. O painel inferior direito é uma representação 3D do local nº 17 mostrando porosidade cortical sobrejacente à cavitação medular. Cortesia do Dr.
Também mencionamos brevemente aqui um dispositivo de ultrassom, o CaviTAU™®, que foi desenvolvido e está sendo usado em partes da Europa, especificamente para detectar áreas de baixa densidade óssea nos maxilares superiores e inferiores que são sugestivas de cavitações ósseas. Este dispositivo de ultrassonografia transalveolar (TAU-n) é potencialmente igual em comparação à TCFC na detecção de defeitos da medula óssea e tem o benefício adicional de expor o paciente a níveis muito mais baixos de radiação. Este dispositivo não está atualmente disponível nos EUA, mas está sob revisão pela Food and Drug Administration dos EUA e pode muito bem ser a principal ferramenta de diagnóstico usada na América do Norte para tratar a CIMJD.
Biomarcadores e exame histológico
Devido à natureza inflamatória das cavitações do maxilar, Lechner e Baehr, 2017 investigaram a possível relação entre citocinas selecionadas e a doença. Uma citocina de particular interesse é “regulada após ativação, expressa e secretada por células T normais” (RANTES). Essa citocina, assim como o fator de crescimento de fibroblastos (FGF)-2, é expressa em maior quantidade em lesões cavitacionais e em pacientes com CIMDJ. A Figura 4, fornecida pelo Dr. Lechner, compara os níveis de RANTES em pacientes com cavitação (barra vermelha, à esquerda) com os níveis em controles saudáveis (barra azul), mostrando níveis que são mais de 25 vezes maiores naqueles com a doença. Lechner et al usam duas abordagens para medir os níveis de citocinas. Uma é medir os níveis de citocinas sistemicamente no sangue (Laboratório de soluções de diagnóstico, EUA.). Um segundo método é fazer uma biópsia diretamente do local doente quando ele for acessado para avaliação por um patologista oral. Infelizmente, neste momento, a amostragem localizada de tecidos requer processamento e envio complexos que ainda não foram alcançados em instalações que não sejam de pesquisa, mas forneceu correlações perspicazes.
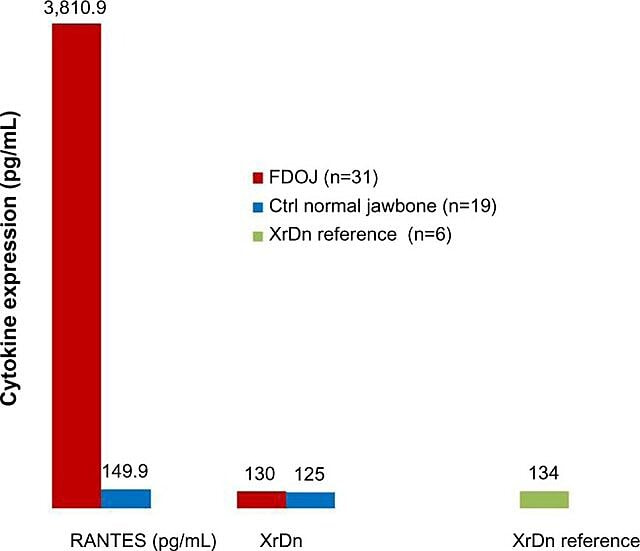
Figura 4 Distribuição da RANTES em 31 casos FDOJ e 19 amostras de mandíbula normal em comparação com uma referência de densidade de raios X para ambos os grupos nas áreas correspondentes. Abreviaturas: RANTES, regulado após ativação, ligante 5 de quimiocina expressa e secretada por células T normais (motivo CC); XrDn, densidade de raios X; FDOJ, osteonecrose gordurosa degenerativa do maxilar; n, número; Ctrl, controle. Figura fornecida pelo Dr. Lechner. Número de licença: CC BY-NC 3.0
Considerações em evolução para fins de diagnóstico
A presença de cavitações ósseas foi bem estabelecida clinicamente. No entanto, diagnósticos claros e parâmetros de tratamento de melhores práticas precisam de mais pesquisas. Com isso em mente, é necessário mencionar brevemente algumas técnicas intrigantes e potencialmente valiosas que estão sendo utilizadas por alguns profissionais.
É reconhecido que avaliações fisiológicas adicionais seriam uma valiosa ferramenta de triagem e diagnóstico. Uma dessas ferramentas usadas por alguns profissionais é a imagem termográfica. A atividade inflamatória generalizada pode ser observada medindo-se os diferenciais de calor na superfície da cabeça e pescoço. A termografia é segura, rápida e pode ter valor diagnóstico semelhante ao da TCFC. Uma desvantagem significativa é a falta de definição, dificultando o discernimento da margem ou extensão de uma lesão.
Avaliação do Meridiano de Acupuntura
Alguns profissionais estão observando o perfil energético de uma lesão utilizando a Avaliação do Meridiano de Acupuntura (AMA) para determinar seu efeito no meridiano de energia correspondente. Este tipo de avaliação é baseada na Eletroacupuntura Segundo Voll (EAV). Esta técnica, que se baseia na antiga medicina chinesa e nos princípios da acupuntura, foi desenvolvida e está sendo ensinada nos EUA. A acupuntura tem sido usada para aliviar a dor e promover a cura. Baseia-se no equilíbrio do fluxo de energia (ou seja, Chi) através de vias específicas de energia no corpo. Esses caminhos, ou meridianos, conectam órgãos, tecidos, músculos e ossos específicos entre si. A acupuntura utiliza pontos muito específicos de um meridiano para influenciar a saúde e a vitalidade de todos os elementos do corpo nesse meridiano. Esta técnica tem sido usada para revelar doenças do maxilar que, quando resolvidas, também tratam doenças aparentemente não relacionadas, como artrite ou síndrome da fadiga crônica. Esta técnica presta-se a uma investigação mais aprofundada (ou seja, os resultados precisam de ser documentados e os dados longitudinais adquiridos e divulgados).
Existem muitos fatores individuais que aumentam o risco de desenvolvimento de cavitações ósseas, mas geralmente o risco é multifatorial. Os riscos para o indivíduo podem ser influências externas, como fatores ambientais, ou influências internas, como função imunológica deficiente. As Tabelas 2 e 3 listam os fatores de risco externos e internos.


Observe que a Tabela 2, Fatores de Risco Internos, não inclui predisposição genética. Embora se pense que as variações genéticas desempenham um papel, nenhuma variação genética única ou mesmo combinação de genes foi identificada como fator de risco, no entanto, influências genéticas são prováveis . Uma revisão sistemática da literatura realizada em 2019 mostrou que vários polimorfismos de nucleotídeo único foram identificados, mas não há replicação entre os estudos. Os autores concluíram que dada a diversidade de genes que mostraram associações positivas com cavitações e a falta de reprodutibilidade dos estudos, o papel desempenhado pelas causas genéticas pareceria moderado e heterogêneo. No entanto, pode ser necessário atingir populações específicas para identificar diferenças genéticas. Na verdade, como foi demonstrado, um dos mecanismos fisiopatológicos mais comuns e básicos do dano ósseo isquêmico é o excesso de coagulação proveniente de estados de hipercoagulação, que geralmente têm bases genéticas, conforme descrito por Bouquot e Lamarche (1999). A Tabela 4 fornecida pelo Dr. Bouquot lista os estados de doença que envolvem hipercoagulação e os próximos 3 parágrafos fornecem uma visão geral de algumas das descobertas do Dr. Bouquot que ele apresentou em sua função como Diretor de Pesquisa no Centro Maxilofacial de Educação e Pesquisa.
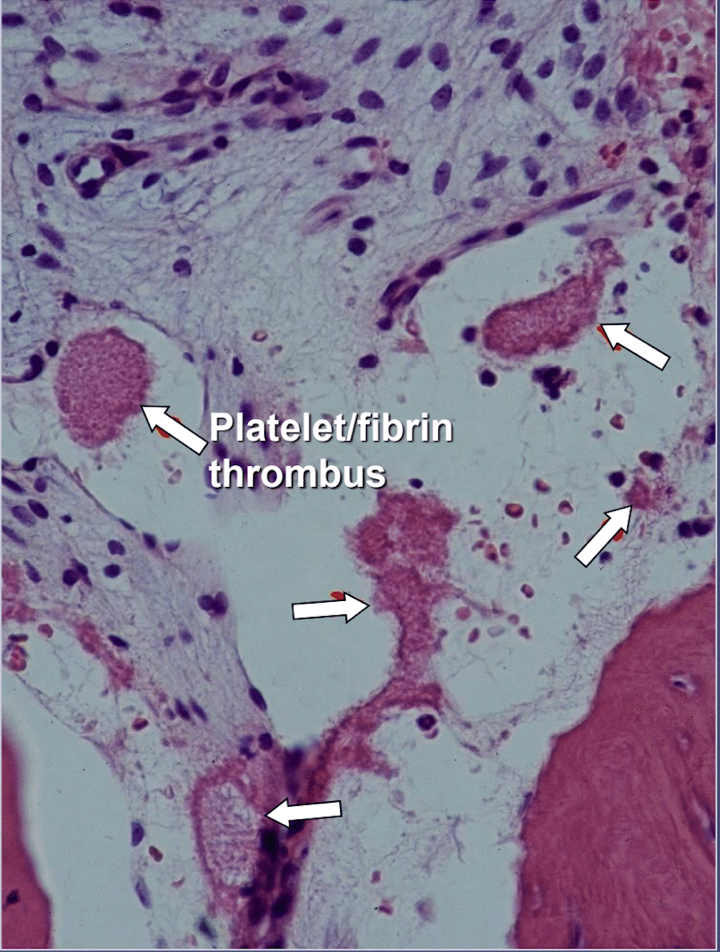
Nas cavitações dos maxilares há evidências claras de osteonecrose isquêmica, que é uma doença da medula óssea em que o osso se torna necrótico devido à privação de oxigênio e nutrientes. Como mencionado, muitos fatores podem interagir para produzir cavitações e até 80% dos pacientes têm um problema, geralmente hereditário, de produção excessiva de coágulos sanguíneos nos vasos sanguíneos. Esta doença normalmente não é revelada durante exames de sangue de rotina. O osso é particularmente suscetível a este problema de hipercoagulação e desenvolve vasos sanguíneos muito dilatados; pressões internas aumentadas, muitas vezes dolorosas; estagnação de sangue; e até infartos. Este problema de hipercoagulação pode ser sugerido por um histórico familiar de acidente vascular cerebral e ataques cardíacos em idade precoce (menos de 55 anos), artroplastia de quadril ou “artrite” (especialmente em idade precoce), osteonecrose (especialmente em idade precoce), profunda trombose venosa, êmbolos pulmonares (coágulos sanguíneos nos pulmões), trombose venosa retiniana (coágulos na retina do olho) e aborto espontâneo recorrente. Os maxilares têm 2 problemas específicos com esta doença: 1) uma vez danificado, o osso doente é pouco capaz de resistir a infecções de baixo grau causadas por bactérias dentárias e gengivais; e 2) o osso pode não se recuperar da diminuição do fluxo sanguíneo induzido pelos anestésicos locais usados pelos dentistas durante o tratamento odontológico. A Figura 5 fornece uma visão microscópica de um trombo intravascular.
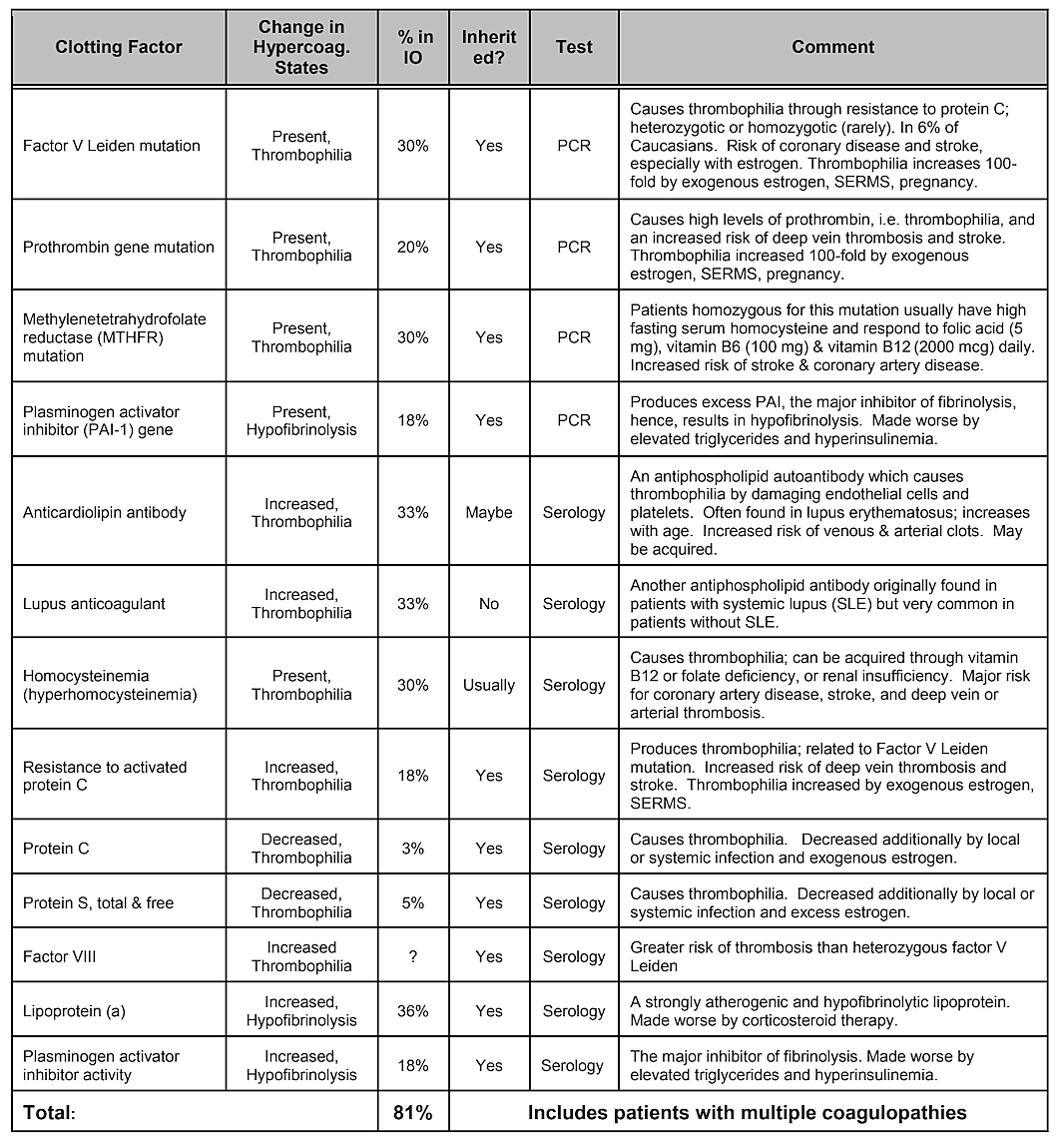
tabela 4 Estados de doença que envolvem hipercoagulação. Quatro em cada cinco pacientes com cavitação óssea maxilar apresentam uma destas coagulações
problemas de fator.
Independentemente da causa subjacente da hipercoagulação, o osso desenvolve uma medula fibrosa (as fibras podem viver em áreas carentes de nutrientes), uma medula gordurosa e morta (“podridão úmida”), uma medula muito seca, às vezes coriácea (“podridão seca”). ), ou um espaço medular completamente oco (“cavitação”).
Qualquer osso pode ser afetado, mas os quadris, joelhos e maxilares são os mais afetados. A dor costuma ser intensa, mas cerca de 1/3rd dos pacientes não sentem dor. O corpo tem dificuldade em curar-se desta doença e 2/3rds dos casos requerem a remoção cirúrgica da medula danificada, geralmente por raspagem com curetas. A cirurgia eliminará o problema (e a dor) em quase 3/4ths dos pacientes com envolvimento da mandíbula, embora cirurgias repetidas, geralmente procedimentos menores que o primeiro, sejam necessárias em 40% dos pacientes, às vezes em outras partes da mandíbula, porque a doença frequentemente apresenta lesões “saltos” (isto é, múltiplos locais na mandíbula). ossos iguais ou semelhantes), com medula normal entre eles. Mais da metade dos pacientes com quadril acabará por desenvolver a doença no quadril oposto. Mais de 1/3rd dos pacientes com mandíbula contrairão a doença em outros quadrantes da mandíbula. Recentemente, descobriu-se que 40% dos pacientes com osteonecrose do quadril ou da mandíbula responderão à anticoagulação com heparina de baixo peso molecular (Lovenox) ou Coumadin com resolução da dor e consolidação óssea.
Figura 5 Visão microscópica de trombos intravasculares
Se estiver procurando uma abordagem não farmacêutica para reduzir o risco de hipercoagulação, pode-se considerar o uso de enzimas suplementares, como a nattoquinase ou a mais potente lumbroquinase, ambas com propriedades fibrinolíticas e anticoagulantes. Além disso, os estados de deficiência de cobre, que estão associados à disfunção da coagulação, devem ser excluídos devido ao risco aumentado de hipercoagulação observado em pacientes com cavitações ósseas maxilares.
IMPLICAÇÕES SISTÊMICAS E CLÍNICAS
A presença de cavitações ósseas e a patologia associada abrangem alguns sintomas específicos, mas também incluem frequentemente alguns sintomas sistémicos inespecíficos. Assim, seu diagnóstico e tratamento devem ser abordados com minuciosa consideração pela equipe assistencial. As realizações mais exclusivas e inovadoras que surgiram desde o documento de posição da IAOMT de 2014 são a resolução de condições inflamatórias crônicas aparentemente não relacionadas após o tratamento de cavitação. Quer as doenças sistêmicas sejam de natureza autoimune ou a inflamação ocorra de outra forma, foram relatadas melhorias significativas, incluindo melhora no câncer. O complexo de sintomas associados a estas lesões é altamente individualizado e, portanto, não generalizável ou facilmente reconhecível. Portanto, a IAOMT acredita que quando um paciente é diagnosticado com cavitações ósseas maxilares com ou sem dor localizada associada, e também tem outra doença sistêmica anteriormente não atribuída a cavitações ósseas maxilares, o paciente precisa de uma avaliação mais aprofundada para determinar se a doença está associada a , ou é uma consequência da doença. A IAOMT entrevistou seus membros para saber mais sobre quais sintomas/doenças sistêmicas são resolvidas após a cirurgia cavitacional. Os resultados são apresentados no Apêndice I.
A presença de citocinas geradas em lesões necróticas e pouco vascularizadas de cavitações ósseas maxilares parece funcionar como foco de citocinas inflamatórias que mantêm outras áreas de inflamação ativas e/ou crônicas. O alívio ou pelo menos a melhora da dor localizada na mandíbula após o tratamento é esperado e esperado, mas esta teoria focal da inflamação, que será discutida em detalhes abaixo, pode explicar por que tantas doenças aparentemente “não relacionadas” que têm ligações com condições inflamatórias crônicas também são diminuídos com o tratamento de cavitação.
Em apoio às conclusões tiradas no documento de posição da IAOMT de 2014, ligando cavitações ósseas maxilares e doenças sistêmicas, pesquisas e estudos clínicos publicados mais recentemente por Lechner, von Baehr e outros mostram que as lesões de cavitação óssea maxilar contêm um perfil específico de citocinas não observado em outras patologias ósseas. . Quando comparadas com amostras de maxilares saudáveis, as patologias de cavitação mostram continuamente uma forte regulação positiva do factor de crescimento de fibroblastos (FGF-2), do antagonista do receptor da interleucina 1 (Il-1ra) e, de particular importância, da RANTES. A RANTES, também conhecida como CCL5 (ligante 5 do motivo cc), foi descrita como uma citocina quimiotática com forte ação pró-inflamatória. Foi demonstrado que estas quimiocinas interferem em vários estágios da resposta imune e estão substancialmente envolvidas em diversas condições patológicas e infecções. Estudos demonstraram que a RANTES está implicada em muitas doenças sistémicas, tais como artrite, síndrome de fadiga crónica, dermatite atópica, nefrite, colite, alopecia, distúrbios da tiróide e na promoção da esclerose múltipla e da doença de Parkinson. Além disso, foi demonstrado que a RANTES causa uma aceleração do crescimento do tumor.
Fatores de crescimento de fibroblastos também foram implicados em cavitações ósseas. Os fatores de crescimento de fibroblastos, FGF-2, e seus receptores associados, são responsáveis por muitas funções cruciais, incluindo proliferação, sobrevivência e migração celular. Eles também são suscetíveis de serem sequestrados por células cancerosas e desempenharem um papel oncogênico em muitos tipos de câncer. Por exemplo, o FGF-2 promove a progressão do tumor e do cancro no cancro da próstata. Além disso, os níveis de FGF-2 mostraram correlação direta com a progressão, metástase e mau prognóstico de sobrevivência em pacientes com câncer colorretal. Em comparação com controlos livres de cancro, os pacientes com carcinoma gástrico apresentam níveis significativamente mais elevados de FGF-2 no soro. Estes mensageiros inflamatórios têm sido implicados em muitas doenças graves, sejam elas de natureza inflamatória ou cancerosas. Em contraste com RANTES/CCL5 e FGF-2, foi demonstrado que o IL1-ra actua como um forte mediador anti-inflamatório, contribuindo para a falta de sinais inflamatórios comuns em algumas lesões de cavitação.
Os níveis excessivos de RANTES e FGF-2 em lesões de cavitação foram comparados e associados aos níveis observados em outras doenças sistêmicas como esclerose lateral amiotrófica, (ELA), esclerose múltipla (EM), artrite reumatóide e câncer de mama. Na verdade, os níveis destes mensageiros detectados nas cavitações dos maxilares são mais elevados do que no soro e no líquido cefalorraquidiano de pacientes com ELA e EM. A pesquisa atual de Lechner e von Baehr demonstrou um aumento de 26 vezes na RANTES nas lesões osteonecróticas do maxilar de pacientes com câncer de mama. Lechner e colegas sugerem que a RANTES derivada da cavitação pode servir como um acelerador do desenvolvimento e progressão do cancro da mama.
Como mencionado anteriormente, existem numerosos casos de cavitações maxilares assintomáticas. Nestes casos, citocinas pró-inflamatórias agudas, como TNF-alfa e IL-6, NÃO são observadas em números aumentados nos achados anatomopatológicos de amostras de cavitação. Nestes pacientes, a ausência dessas citocinas pró-inflamatórias está associada a níveis elevados de uma citocina antiinflamatória antagonista do receptor de interleucina 1 (Il-1ra). A conclusão razoável é que a inflamação aguda associada às cavitações do maxilar está sob o controlo de níveis elevados de RANTES/FGF-2. Como resultado, para fazer um diagnóstico, Lechner e von Baehr sugerem não enfatizar o foco na presença de inflamação e considerar a via de sinalização, principalmente através da superexpressão de RANTES/FGF-2. Os elevados níveis de RANTES/FGF-2 em pacientes com cavitação indicam que estas lesões podem estar a causar vias de sinalização patogénica semelhantes e que se reforçam mutuamente para outros órgãos. O sistema imunológico é ativado em resposta a sinais de perigo, que evocam várias vias moleculares inatas que culminam na produção de citocinas inflamatórias e na possível ativação do sistema imunológico adaptativo. Isto apoia a ideia e a teoria de que as cavitações ósseas do maxilar podem servir como uma causa fundamental de doenças inflamatórias crónicas através da produção de RANTES/FGF-2 e explica ainda por que os sintomas agudos de inflamação nem sempre são vistos ou sentidos pelo paciente nas lesões do maxilar. eles mesmos. Assim, as cavitações do maxilar e estes mensageiros implicados representam um aspecto integrativo da doença inflamatória e servem como uma etiologia potencial da doença. A remoção de cavitações pode ser a chave para reverter doenças inflamatórias. Isto é apoiado pela observação de uma redução nos níveis séricos de RANTES pós-intervenção cirúrgica em 5 pacientes com cancro da mama (ver Tabela 5). Mais pesquisas e testes dos níveis da RANTES/CCL5 podem fornecer informações sobre esta relação. As observações encorajadoras são as melhorias na qualidade de vida obtidas por muitos pacientes com cavitação óssea maxilar, seja através do alívio no local da operação ou da diminuição da inflamação crónica ou de doenças noutros locais.
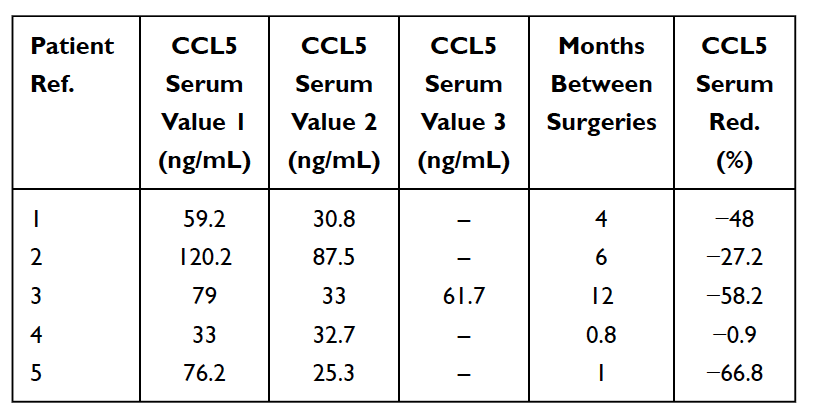
tabela 5
Redução (Red.) em RANTES/CCL5 no soro em 5 pacientes com câncer de mama submetidos à cirurgia para osteonecrose degenerativa gordurosa do maxilar (FDOJ). Tabela adaptada de
Lechner et al, 2021. Cavitação do maxilar expressa RANTES/CCL5: Estudos de caso que ligam a inflamação silenciosa no maxilar à epistemologia do cancro da mama.” Câncer de mama: alvos e terapia.
Devido à escassez de literatura sobre o tratamento de lesões cavitacionais, a IAOMT pesquisou os seus membros para reunir informações sobre quais tendências e tratamentos estão se desenvolvendo em direção a um “padrão de atendimento”. Os resultados da pesquisa são discutidos brevemente no Apêndice II.
Uma vez determinados a localização e o tamanho das lesões, são necessárias modalidades de tratamento. A IAOMT acredita que geralmente é inaceitável deixar “osso morto” no corpo humano. Isto se baseia em dados que sugerem que as cavitações dos maxilares podem ser o foco de citocinas e endotoxinas sistêmicas para iniciar o processo de degradação da saúde geral do paciente.
Em circunstâncias ideais, uma biópsia deve ser realizada para confirmar o diagnóstico de qualquer patologia do maxilar e descartar outros estados de doença. Então, é necessário um tratamento para remover ou eliminar a patologia envolvida e estimular o crescimento do osso normal e vital. Neste momento, na literatura revisada por pares, a terapia cirúrgica que consiste na excisão do osso não vital afetado parece ser o tratamento preferido para cavitações ósseas maxilares. O tratamento envolve o uso de anestésicos locais, o que leva a uma consideração importante. Anteriormente, pensava-se que os anestésicos contendo epinefrina, que possuem propriedades vasoconstritoras conhecidas, deveriam ser evitados em pacientes que já pudessem ter comprometimento do fluxo sanguíneo associado ao seu estado de doença. Contudo, numa série de estudos moleculares, a diferenciação osteoblástica aumentou com o uso de epinefrina. Portanto, o médico deve determinar caso a caso se deve usar epinefrina e, em caso afirmativo, a quantidade que deve ser utilizada para obter os melhores resultados.
Após uma decorticação cirúrgica e curetagem completa da lesão e irrigação com solução salina normal estéril, a cicatrização é melhorada pela colocação de enxertos de fibrina rica em plaquetas (PRF) no vazio ósseo. O uso de concentrados de fibrina ricos em plaquetas em procedimentos cirúrgicos não é benéfico apenas do ponto de vista da coagulação, mas também do aspecto da liberação de fatores de crescimento durante um período de até quatorze dias após a cirurgia. Antes do uso de enxertos PRF e outras terapias adjuvantes, a recidiva da lesão osteonecrótica do maxilar após a cirurgia ocorria em até 40% dos casos.
Uma análise dos fatores de risco externos descritos na Tabela 2 sugere fortemente que resultados desfavoráveis podem ser evitados com técnica cirúrgica apropriada e interação médico/paciente, especialmente em populações suscetíveis. É aconselhável considerar a adoção de técnicas atraumáticas, minimizando ou prevenindo doenças periodontais e outras doenças dentárias, e escolhendo um arsenal que permita os melhores resultados de cura. Fornecer instruções completas pré e pós-operatórias ao paciente, incluindo os riscos associados ao fumo, pode ajudar a minimizar os resultados negativos.
Tendo em mente a ampla lista de potenciais fatores de risco listados nas Tabelas 2 e 3, recomenda-se consultas com a equipe de atendimento ampliado do paciente para determinar adequadamente quaisquer possíveis fatores de risco ocultos que possam contribuir para o desenvolvimento de cavitações ósseas maxilares. Por exemplo, uma consideração importante no tratamento de cavitações maxilares é se o indivíduo está tomando antidepressivos, especificamente inibidores seletivos da recaptação de serotonina (ISRS). Os ISRS têm sido associados à redução da densidade da massa óssea e ao aumento das taxas de fraturas. O ISRS Fluoxetina (Prozac) inibe diretamente a diferenciação e mineralização dos osteoblastos. Pelo menos dois estudos independentes que examinaram usuários de ISRS em comparação com controles mostraram que o uso de ISRS está associado a piores índices morfométricos panorâmicos.
O pré-condicionamento também pode contribuir para resultados bem-sucedidos do tratamento. Isto envolve a criação de um ambiente tecidual propício à cura, fornecendo ao corpo níveis adequados de nutrientes apropriados que melhoram o terreno biológico, otimizando a homeostase do corpo. As táticas de pré-condicionamento nem sempre são possíveis ou aceitáveis para o paciente, mas são mais importantes para aqueles pacientes que têm suscetibilidades conhecidas, como aqueles com predisposição genética, distúrbios de cura ou saúde comprometida. Nesses casos, é fundamental que essa otimização ocorra para minimizar os níveis de estresse oxidativo, que pode não só estimular o processo da doença, mas também interferir na cura desejada.
Idealmente, a redução de qualquer carga tóxica no corpo, como flúor e/ou mercúrio, proveniente de obturações de amálgama dentária, deve ser concluída antes do tratamento das cavitações dos maxilares. O mercúrio pode deslocar o ferro na cadeia de transporte de elétrons das mitocôndrias. Isto resulta em excesso de ferro livre (ferro ferroso ou Fe++), produzindo espécies reativas de oxigênio (ROS) prejudiciais, também conhecidas como radicais livres, que causam estresse oxidativo. O excesso de ferro no tecido ósseo também inibe o bom funcionamento dos osteoblastos, o que obviamente terá um efeito negativo ao tentar curar uma doença óssea.
Outras deficiências também devem ser tratadas antes do tratamento. Quando há deficiência de cobre, magnésio e retinol biodisponíveis, o metabolismo e a reciclagem do ferro ficam desregulados no corpo, o que contribui para o excesso de ferro livre nos locais errados, levando a um estresse oxidativo ainda maior e ao risco de doenças. Mais especificamente, muitas enzimas no corpo (como a ceruloplasmina) tornam-se inativas quando há níveis insuficientes de cobre, magnésio e retinol biodisponíveis, o que perpetua a desregulação sistêmica do ferro e o resultante aumento do estresse oxidativo e do risco de doenças.
Estratégias alternativas de tratamento
Técnicas alternativas utilizadas como terapias primárias ou de suporte também devem ser avaliadas. Isso inclui homeopatia, estimulação elétrica, terapia de luz, como fotobiomodulação, e laser, oxigênio/ozônio de grau médico, oxigênio hiperbárico, modalidades de anticoagulação, remédios Sanum, nutrição e nutracêuticos, sauna infravermelha, ozonioterapia intravenosa, tratamentos energéticos e outros. Neste momento, não foi realizada ciência que confirme que estas formas alternativas de tratamento são viáveis ou ineficazes. Devem ser estabelecidos padrões de cuidados para garantir a cura e desintoxicação adequadas. As técnicas para avaliar o sucesso devem ser testadas e padronizadas. Protocolos ou procedimentos para ajudar a determinar quando o tratamento é apropriado e quando não é devem ser apresentados para avaliação.
A pesquisa mostrou que a presença de cavitações nos maxilares é um processo de doença insidioso associado à redução do fluxo sanguíneo. O fluxo sanguíneo medular comprometido leva a uma vascularização pouco mineralizada e inadequada em áreas do maxilar que podem ser infectadas com patógenos, aumentando a morte celular. O fluxo sanguíneo lento dentro das lesões cavitacionais desafia a entrega de antibióticos, nutrientes e mensageiros imunológicos. O ambiente isquêmico também pode abrigar e promover mediadores inflamatórios crônicos que podem ter efeitos ainda mais deletérios na saúde sistêmica. A predisposição genética, a função imunológica reduzida, os efeitos de certos medicamentos, traumas e infecções e outros fatores como o tabagismo podem instigar ou acelerar o desenvolvimento de cavitações ósseas.
Juntamente com o eminente patologista maxilar, Dr. Jerry Bouquot, a IAOMT está apresentando e promovendo uma identificação histológica e patologicamente correta de lesões cavitacionais do maxilar como Doença Medular Isquêmica Crônica do Maxilar, CIMDJ. Embora muitos nomes, siglas e termos tenham sido usados historicamente e atualmente sejam usados para denotar esta doença, a IAOMT está convencida de que este é o termo mais apropriado para descrever a condição patológica e micro-histológica comumente encontrada nas cavitações ósseas maxilares.
Embora a maioria das lesões cavitacionais da mandíbula sejam difíceis de diagnosticar com radiografias de rotina e a maioria não seja dolorosa, nunca se deve presumir que o processo da doença não existe. Existem muitos processos patológicos que são difíceis de diagnosticar e muitos que não são dolorosos. Se utilizássemos a dor como indicador de tratamento, a doença periodontal, a diabetes e a maioria dos cancros não seriam tratados. O dentista de hoje tem um amplo espectro de modalidades para tratar com sucesso as cavitações dos maxilares e a falha em reconhecer a doença e recomendar o tratamento não é menos grave do que a falha no diagnóstico e tratamento da doença periodontal. Para a saúde e o bem-estar dos nossos pacientes, é crucial uma mudança de paradigma para todos os profissionais de saúde, incluindo médicos e dentistas, para 1) reconhecerem a prevalência de cavitações ósseas maxilares e 2) reconhecerem a ligação entre cavitações ósseas maxilares e doenças sistémicas.
RESULTADOS DA PESQUISA IAOMT 2 (2023)
Conforme discutido brevemente no artigo, condições não relacionadas geralmente remitem após a cirurgia de cavitação. Para saber mais sobre quais tipos de condições são resolvidas e como ocorre a remissão proximal em relação à cirurgia, uma segunda pesquisa foi enviada aos membros da IAOMT. Uma lista de sintomas e condições que os membros deste comitê observaram melhorar após a cirurgia foi compilada para a pesquisa. Os entrevistados foram questionados se haviam observado remissão de alguma dessas condições após a cirurgia e, em caso afirmativo, em que grau. Eles também foram questionados se os sintomas regrediram rapidamente ou se as melhorias demoraram mais de dois meses. Além disso, os entrevistados foram questionados se normalmente realizavam cirurgias em locais individuais, em múltiplos locais unilaterais ou em todos os locais em uma cirurgia. Os resultados da pesquisa são apresentados nas Figuras abaixo. Os dados são preliminares, dado que o número de entrevistados foi pequeno (33) e que há alguns dados faltantes.
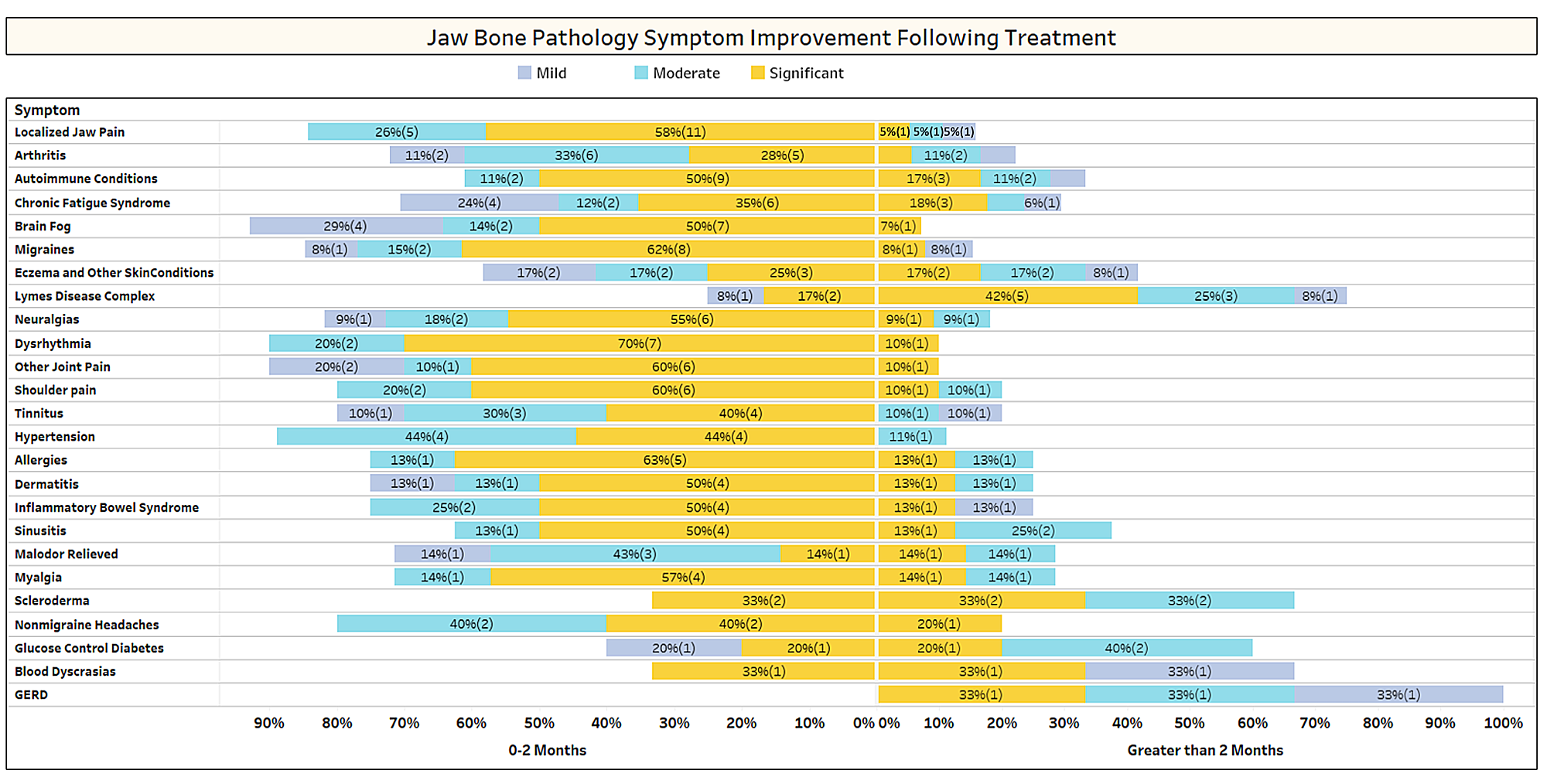
Apx I Fig 1 Os entrevistados avaliaram o nível de melhoria (leve, moderada ou significativa) e observaram se a melhoria ocorreu rapidamente (0-2 meses) ou demorou mais (> 2 meses). As condições/sintomas estão listadas na ordem em que são mais relatadas. Observe que a maioria das condições/sintomas regrediram em menos de dois meses (lado esquerdo da linha média).
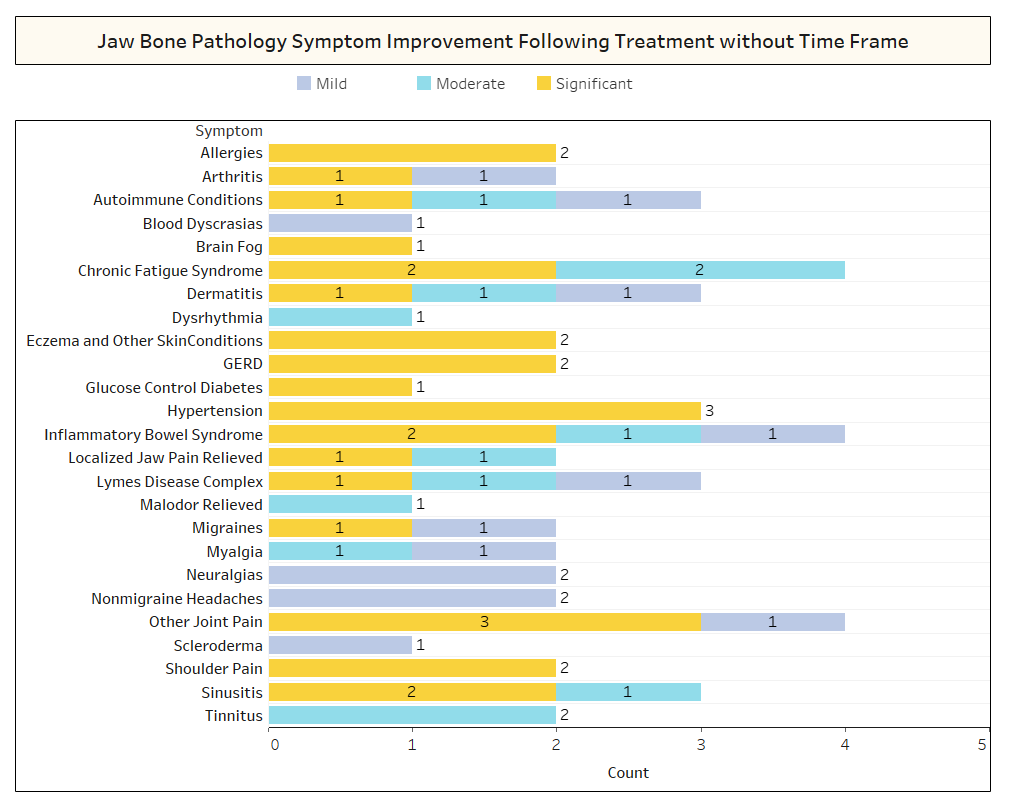
Apx I Fig 2 Conforme mostrado acima, em vários casos, os entrevistados não observaram o prazo de recuperação das melhorias observadas.
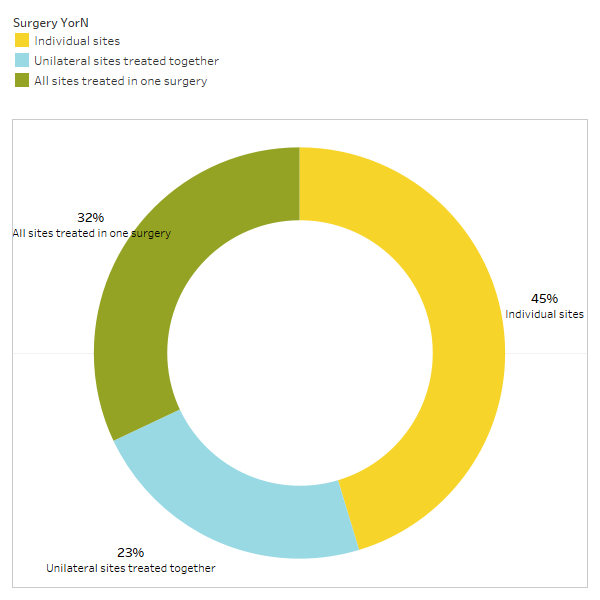
Apx I Fig 3 Os entrevistados responderam à pergunta: “Você normalmente recomenda/realiza
uma cirurgia para locais individuais, locais unilaterais tratados em conjunto ou todos os locais tratados em uma cirurgia?”
RESULTADOS DA PESQUISA IAOMT 1 (2021)
Devido à escassez de literatura e de revisões de casos clínicos relacionados com o tratamento de lesões cavitacionais, a IAOMT pesquisou os seus membros para recolher informações sobre quais as tendências e tratamentos que estão a desenvolver-se em direcção a um “padrão de cuidados”. A pesquisa completa está disponível no site da IAOMT (observe que nem todos os profissionais responderam a todas as perguntas da pesquisa).
Para resumir brevemente, a maioria dos 79 entrevistados oferece tratamento cirúrgico, que envolve reflexão dos tecidos moles, acesso cirúrgico ao local da cavitação e vários métodos de “limpeza” física e desinfecção do local afetado. Uma ampla gama de medicamentos, nutracêuticos e/ou hemoderivados são usados para promover a cicatrização da lesão antes do fechamento da incisão nos tecidos moles.
Fresas rotativas são frequentemente usadas para abrir ou acessar a lesão óssea. A maioria dos médicos utiliza um instrumento manual para curetar ou raspar o osso doente (68%), mas outras técnicas e ferramentas também são utilizadas, como uma broca rotativa (40%), um instrumento piezoelétrico (ultrassônico) (35%) ou um Laser ER:YAG (36%), que é uma frequência de laser usada para streaming fotoacústico.
Depois que o local é limpo, desbridado e/ou curetado, a maioria dos entrevistados usa água/gás de ozônio para desinfetar e promover a cura. 86% dos entrevistados utilizam PRF (fibrina rica em plaquetas), PRP (plasma rico em plaquetas) ou PRF ou PRP ozonizado. Uma técnica de desinfecção promissora relatada na literatura e nesta pesquisa (42%) é o uso intraoperatório de Er:YAG. 32% dos entrevistados não utilizam nenhum tipo de enxerto ósseo para preencher o local da cavitação.
A maioria dos entrevistados (59%) normalmente não faz biópsia das lesões, alegando uma variedade de razões, desde custo, incapacidade de obter amostras de tecido viáveis, dificuldade em encontrar um laboratório de patologia ou certeza do estado da doença.
A maioria dos entrevistados não utiliza antibióticos no pré-operatório (79%), durante a cirurgia (95%) ou no pós-operatório (69%). Outro suporte intravenoso usado inclui esteróides dexametasona (8%) e vitaminas C (48%). Muitos entrevistados (52%) utilizam terapia a laser de baixa intensidade (LLLT) no pós-operatório para fins de cura. Muitos entrevistados recomendam suporte nutricional, incluindo vitaminas, minerais e vários medicamentos homeopáticos antes (81%) e durante (93%) o período de cura.
 Imagens
Imagens
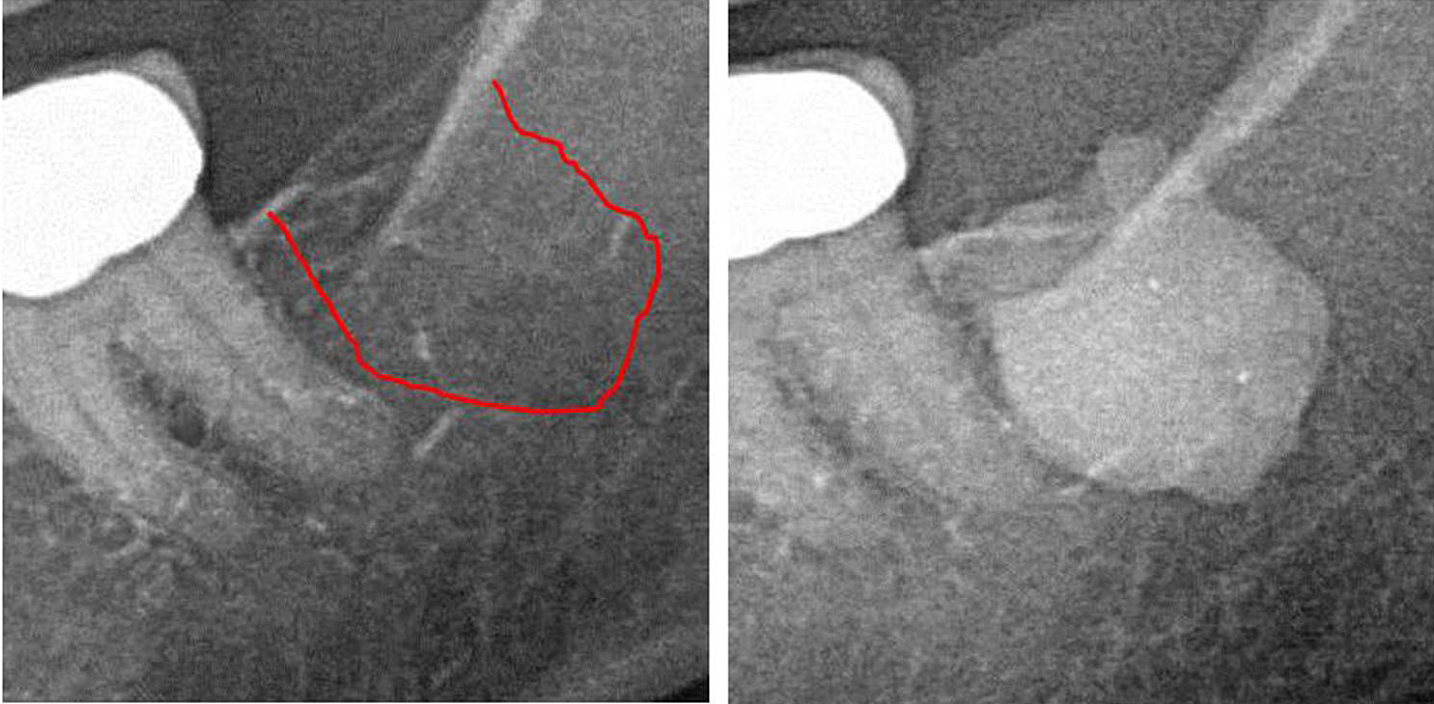
Anexo III Figura 1 Painel esquerdo: diagnóstico de raios X 2D da área #38. Painel direito: Documentação da extensão do FDO) na área retromolar 38/39 usando agente de contraste após cirurgia de FDOJ.
Abreviaturas: FDOJ, osteonecrose degenerativa gordurosa do maxilar.
Adaptado de Lechner, et al, 2021. “Cavitação do maxilar expressa RANTES/CCL5: estudos de caso que ligam a inflamação silenciosa no maxilar à epistemologia do cancro da mama”. Câncer de mama: alvos e terapia
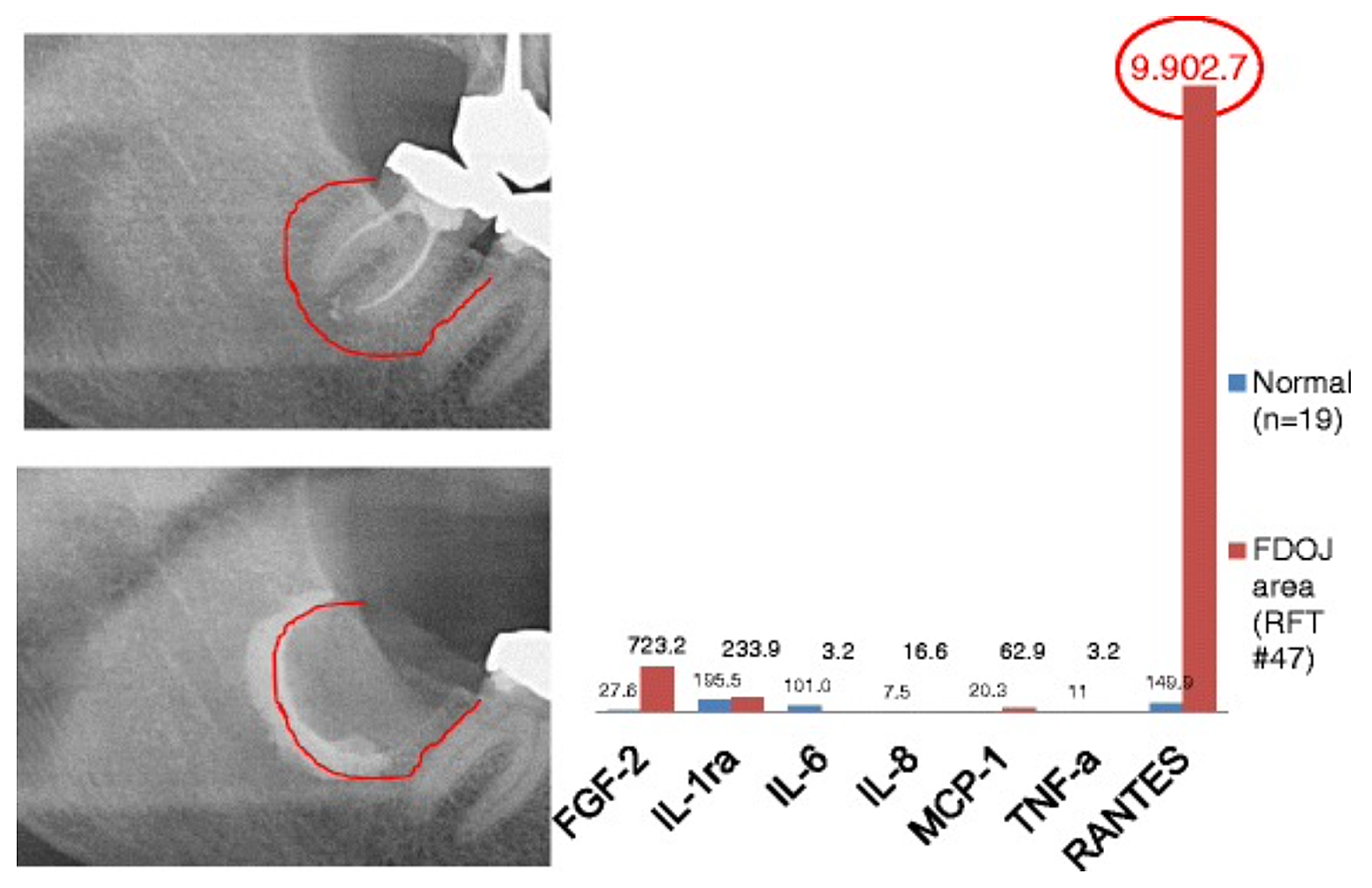
Anexo 3 Figura 2 Comparação de sete citocinas (FGF-2, IL-1ra, IL-6, IL-8, MCP-1, TNF-a e RANTES) no FDOJ abaixo do RFT #47 com as citocinas no maxilar saudável (n = 19). Documentação intraoperatória da extensão do FDOJ no maxilar inferior direito, área #47 apical do RFT #47, por agente de contraste após a remoção cirúrgica do RFT #47.
Abreviaturas: FDOJ, osteonecrose degenerativa gordurosa do maxilar.
Adaptado de Lechner e von Baehr, 2015. “A quimiocina RANTES/CCL5 como uma ligação desconhecida entre a cicatrização de feridas no maxilar e a doença sistêmica: a previsão e os tratamentos personalizados estão no horizonte?” A Revista EPMA
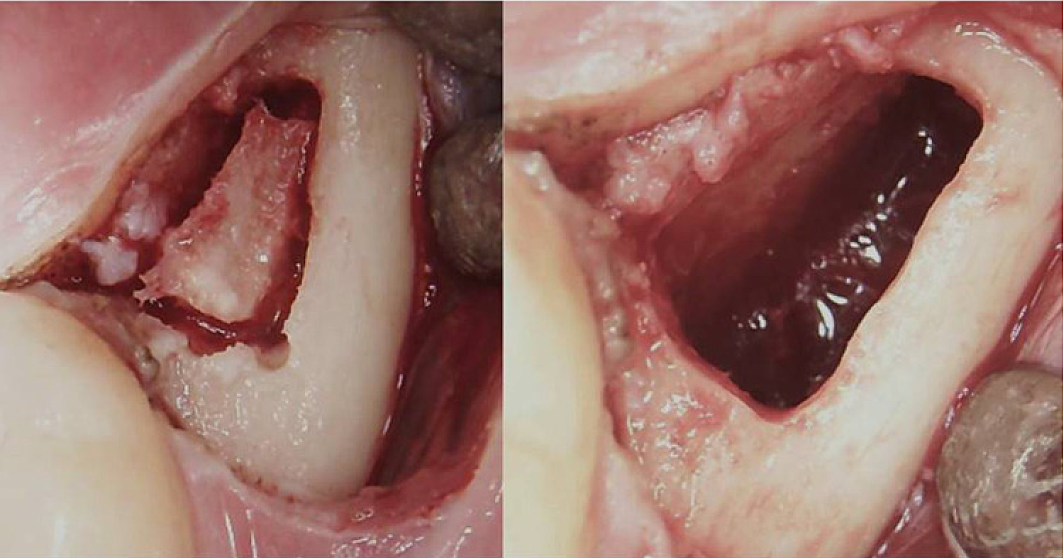
Anexo III Figura 3 Procedimento cirúrgico para BMDJ/FDOJ retromolar. Painel esquerdo: após dobrar o retalho mucoperiosteal, formou-se uma janela óssea na cortical. Painel direito: cavidade medular curetada.
Abreviaturas: BMDJ, defeito da medula óssea no maxilar; FDOJ, osteonecrose degenerativa gordurosa do maxilar.
Adaptado de Lechner, et al, 2021. “Síndrome de fadiga crônica e defeitos da medula óssea da mandíbula – um relato de caso sobre diagnósticos adicionais de raios-X odontológicos com ultrassom”. Jornal internacional de relatos de casos médicos
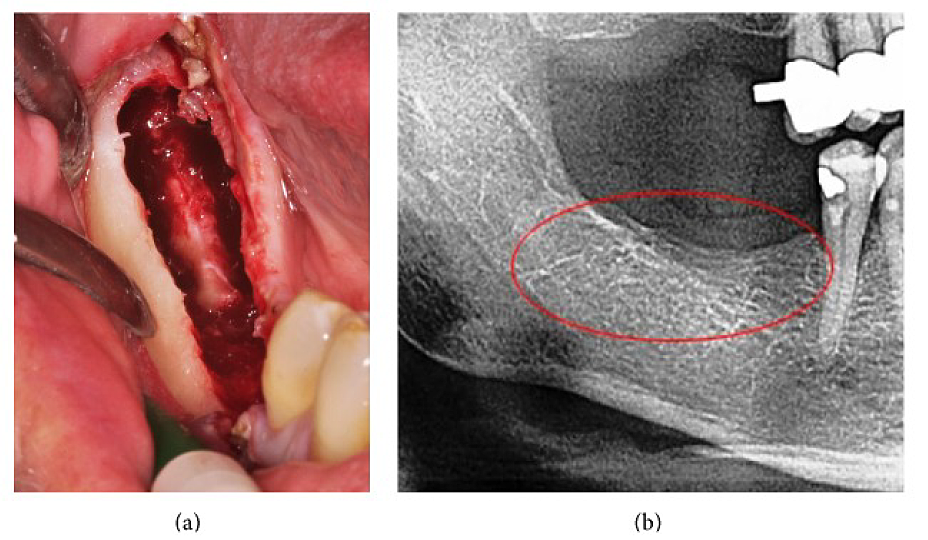
Anexo III Figura 4 (a) Curetagem de FDOJ na mandíbula com nervo infra-alveolar desnudado. (b) Radiografia correspondente sem quaisquer sinais de processo patológico no maxilar.
Abreviaturas: FDOJ, osteonecrose degenerativa gordurosa do maxilar
Adaptado de Lechner, et al, 2015. “Dor facial neuropática periférica/trigeminal e RANTES/CCL5 na cavitação do maxilar”. Baseada em Evidências Medicina Complementar e Alternativa
Appx III Filme 1
Videoclipe (clique duas vezes na imagem para ver o clipe) de cirurgia do maxilar mostrando glóbulos de gordura e secreção purulenta do maxilar de um paciente com suspeita de necrose do maxilar. Cortesia do Dr.
Appx III Filme 2
Videoclipe (clique duas vezes na imagem para ver o clipe) de cirurgia do maxilar mostrando glóbulos de gordura e secreção purulenta do maxilar de um paciente com suspeita de necrose do maxilar. Cortesia do Dr.
Para baixar ou imprimir esta página em um idioma diferente, escolha primeiro seu idioma no menu suspenso no canto superior esquerdo.
Documento de posição da IAOMT sobre autores de cavitações do maxilar humano













